Komentarz do artykułu: Wykrywanie i monitorowanie zakażeń pneumokokowych - wytyczne WHO
Komentarz
dr n. med. Jacek Mrukowicz
Redaktor Naczelny „Medycyny Praktycznej – Szczepienia”
Polski Instytutu Evidence-Based Medicine w Krakowie
Małgorzata Ściubisz, mgr zdrowia publicznego
redaktor „Medycyny Praktycznej Szczepienia”
Komentowane wytyczne (standard) WHO zawierają wiele
istotnych informacji nie tylko dla decydentów i instytucji
zdrowia publicznego nadzorujących program szczepień
ochronnych (PSO) oraz epidemiologię inwazyjnej choroby
pneumokokowej (IChP) lub innych inwazyjnych zakażeń
bakteryjnych w Polsce, ale także dla rzeszy lekarzy
praktyków i mikrobiologów klinicznych, którzy pracują
na „pierwszej linii frontu” i od których – w decydującym
stopniu – zależy czułość systemu nadzoru epidemiologicznego,
czyli skuteczność w identyfikacji przypadków
zakażeń inwazyjnych.1
Odpowiednio przedstawione i zinterpretowane dane z nadzoru epidemiologicznego mogą być ważnym elementem
wspomagającym decyzje w zakresie realizacji i modyfikacji PSO, na przykład takich jak:
- konieczność wprowadzenia szczepień i ustalenia populacji, która zostanie nimi objęta (niemowlęta i małe dzieci, szczepienia wychwytujące dla dzieci starszych, dorośli ≥65. rż., grupy ryzyka z uwagi na stan zdrowia)
- wybór szczepionki
- monitorowanie efektów programu szczepień
- modyfikacja programu szczepień (np. zmiana schematu szczepienia, grup i populacji objętych szczepieniami, zmiana rodzaju szczepionki).
Ważne jest jednak, aby dane z nadzoru były jak najlepszej jakości (wiarygodności), a ich interpretacja i zakres wykorzystania do wspomagania decyzji uwzględniał ich jakość. W innym przypadku decyzje w zakresie zdrowia publicznego będą chybione, a środki publiczne nie zostaną wykorzystane efektywnie (tzn. zwiększenie wydatków nie przyniesie określonej dodatkowej korzyść zdrowotnej dla pacjentów i społeczeństwa). Wydaje nam
się, że ten aspekt niestety umyka w toczącej się u nas dyskusji nad efektami szczepień przeciwko pneumokokom, mimo iż jest bardzo istotny.
Na znaczenie nadzoru epidemiologicznego nad IChP, w tym jakości danych i sposobu ich interpretacji, zwrócono
uwagę w najnowszym stanowisku WHO dotyczącym
szczepień przeciwko pneumokokom.2 Im większa
jest czułość systemu (zdolność do wykrywania chorych
na IChP), im bardziej kompletne są zgłoszenia i dane, a jakość metodologiczna nadzoru, analizy oraz prezentacji
danych lepsza i zgodna z zaleceniami, tym większa
pewność, że obserwowane zmiany odzwierciedlają
rzeczywiste zjawiska, a nie są wynikiem przypadku lub
wpływu istotnych czynników zakłócających lub błędów
systematycznych. Dotyczy to zwłaszcza tak podatnych
na te wpływy parametrów, jakimi są zmiana proporcji
poszczególnych serotypów (zjawisko tzw. zastępowania
serotypów) i próba jej korelacji z efektami programu
szczepień PCV oraz zjawisko ochrony zbiorowiskowej
(pośredniej).
Nawet najprostszy, podstawowy system nadzoru epidemiologicznego
jest przydatny, trzeba jednak znać
jego ograniczenia i możliwości, aby nie interpretować i nie wykorzystywać uzyskanych danych w sposób
nieuprawniony. W tym celu należy regularnie oceniać
jego funkcjonowanie i jakość, publikować wyniki tych
ocen i dążyć do jego poprawy. W komentarzu pragniemy
zwrócić uwagę na kilka problemów związanych z tym
zagadnieniem, które są istotne w polskich warunkach.
Wykrywalność IChP i czułość nadzoru – wskazówki dla lekarzy
Nie bez powodu na wstępie komentarza zwróciliśmy uwagę na czułość systemu nadzoru i kluczową rolę lekarzy praktyków w wykrywaniu zachorowań. Polski system nadzoru epidemiologicznego nad IChP, wprowadzony i koordynowany przez centralne laboratorium Krajowego Ośrodka Referencyjnego ds. Diagnostyki Bakteryjnych Zakażeń Ośrodkowego Układu Nerwowego (KOROUN) w Warszawie, od wielu lat boryka się bowiem z problemem małej wykrywalności IChP. To samo dotyczy systemu obowiązkowego zgłaszania zachorowań na choroby zakaźne koordynowanego przez Zakład Epidemiologii Narodowego Instytutu Zdrowia Publicznego–Państwowego Zakładu Higieny (NIZP–PZH). Współczynniki zapadalności na IChP w wielu innych krajach Europy i Stanach Zjednoczonych – zarówno z okresu przed wprowadzeniem programu szczepień dzieci szczepionkami skoniugowanymi (PCV), jak i aktualnie – są kilka–kilkanaście razy większe niż w Polsce (tab. I).3-22 Taka słaba wykrywalność lub zgłaszalność zachorowań na IChP w Polsce drastycznie ogranicza możliwość wykorzystania danych z nadzoru do oceny efektów prowadzonego programu szczepień (p. niżej). Sytuacja stopniowo się poprawia, ale niestety bardzo wolno (tab. II). Według opublikowanych raportów w 2017 i 2018 roku do KOROUN przesłano odpowiednio 870 i 1037 izolatów z całej populacji (ponad 38 mln mieszkańców), z czego od dzieci odpowiednio: 33 i 32 (<2. rż.) oraz 18 i 48 (2.–4. rż.) izolatów.22 Jakie są prawdopodobne przyczyny małej wykrywalności IChP w Polsce?
| Tabela I. Zachorowalność na inwazyjną chorobę pneumokokową (liczba przypadków/100 000/rok) w wybranych krajach przed wprowadzeniem programu szczepień dzieci i aktualnie | ||||||
|---|---|---|---|---|---|---|
| Kraj | Populacja (wiek) | Zapadalność przed PCV (rok) | Zapadalność aktualnie (rok)a | Rodzaj stosowanych szczepionek | Czas realizacji programu szczepień (lata)b | Piśmiennictwo (nr) |
| USA | ogólnac | 24,4 (1999) | 9,5 (2017) | PCV-7 ⇒ PCV-13 | 19 lat | 3, 4, 5 |
| <5. rż. | 87,4 (1999) | 7 (2017) | ||||
| Wielka Brytania | ogólna | 14,79 (2000–2006) | 9,87 (2016–2017) | PCV-7 ⇒ PCV-13 | 14 lat | 6 |
| <2 lat 2–4 lat | 49,0 15,31 (2000–2006) | 13,9 4,02 (2016–2017) | ||||
| Niemcy | ≥60 lat | 1,6 (2003–2006) | 10,0 (2017–2018) | PCV-7 ⇒ PCV-13 | 14 lat | 7, 8 |
| <2 lat 2–4 lat | 11,09 3,2 (2003–2006) |
5,94 1,4 (2017–2018) | ||||
| Francja | ogólna | 9,6 (2002) | 7,9 (2017) | PCV-7 ⇒ PCV-13 | 17 lat | 9, 10, 11, 12 |
| <5 lat <2 lat 2–4 lat |
18,0 (1998–2003) 32,7/100 000 (1998–2002) 10,5/100 000 (2008–2009)d | 12,1 (2010–2013) 16,6/100 000 (2017) 4,6/100 000 (2017) | ||||
| Holandia | ogólna | 16,06 (2004–2006) | 15,18 (2016–2018) | PCV-7 ⇒ PCV-10 | 14 lat | 13 |
| <5. rż. | 19,82 (2004–2006) | 6,18 (2016–2018) | ||||
| Finlandia | ogólna | 15,5 (2009) | 14,9 (2017) | PCV-10 | 10 lat | 14, 15 |
| <2 lat 2–4 lat | 51,9 22,9 (2009) | 14,1 8,5 (2017) | ||||
| Austria | ogólna | 1,9 (2011) | 5,0 (2016) | PCV-10 | 8 lat | 11, 16, 17 |
| <5. rż.e | 7,63 (2009–2011) | 4,95 (2015–2016) | ||||
| Polska | ogólna | 2,51 (2016) | 3,52 (2018) | PCV-10 | 3 lata | 18, 19, 20, 21 |
| <2 lat 2–4 lat | 5,43 2,34 (2016) | 4,11 4,29 (2018) | ||||
| a ostatnia oficjalna publikacja b czas realizacji programu do 2019 r. włącznie c dodatkowo PCV-13 zalecana dla osób dorosłych ≥65. rż. od 2014 r. d ostatnie lata prowadzenia programu powszechnych szczepień z użyciem PCV-7; od 2010 r. stosowano PCV-13 e względnie mały odsetek zaszczepionych dzieci przez większość lat realizacji programu (w latach 2012–2016 odpowiednio 18,2%, 30,7%, 42%, 54,5% i 62,6% dzieci <5. rż. otrzymało ≥2 dawki szczepionki) | ||||||
| Tabela II. Liczba izolatów i odsetek przypadków IChP w całej populacji Polski potwierdzonej metodą PCR w latach 2010–2018 przez KOROUNa | ||
|---|---|---|
| Rok | Liczba izolatów ogółem | Liczba (%) przypadków potwierdzonych PCRb |
| 2018 | 1037 | 28 (2,7) |
| 2017 | 870 | 18 (2,1) |
| 2016 | 699 | 21 (3,0) |
| 2015 | 701 | 30 (4,3) |
| 2014 | 555 | 20 (3,6) |
| 2013 | 474 | 21 (4,4) |
| 2012 | 365 | 16 (4,4) |
| 2011 | 355 | 17 (4,8) |
| 2010 | 298 | 30 (10,1) |
| a na podstawie 22. pozycji piśmiennictwa; populacja Polski w 2018 r.: 38 411 000 (wg
Głównego Urzędu Statystycznego) b pozostałe przypadki potwierdzone metodami hodowlanymi (posiew) IChP – inwazyjna choroba pneumokokową, PCR – łańcuchowa reakcja polimerazy | ||
1. Czujność diagnostyczna – należy badać wszystkich chorych spełniających kryteria kliniczne. Jednym z parametrów dobrej jakości nadzoru według WHO jest pobieranie przez lekarzy próbek do badań bakteriologicznych i ich wykonywanie u ≥80% chorych z podejrzeniem inwazyjnej choroby bakteryjnej. Wydaje się, że w naszych warunkach ten etap w istotnym stopniu przyczynia się do małej wykrywalności IChP. Kluczem do poprawienia sytuacji jest świadomość i organizacyjne możliwości lekarzy pracujących na oddziałach szpitalnych i SOR, aby wymienione przez WHO badania bakteriologiczne traktować jako rutynowy element postępowania w każdym uzasadnionym klinicznie podejrzeniu IChP. Podane przez WHO kryteria (objawy) kliniczne podejrzenia ZOMR, sepsy i ciężkiego zapalenia płuc (p. Kryteria kliniczne ZOMR w celu klasyfikacji przypadku, Kryteria kliniczne zapalenia płuc w celu klasyfikacji przypadku oraz Kryteria kliniczne sepsy w celu klasyfikacji przypadku) pomagają wyłapać takich chorych, a opisane zasady pobierania i przesyłania materiału diagnostycznego przypominają, jak to zrobić poprawnie, aby zwiększyć szansę wykrycia patogenu (p. Postępowanie diagnostyczne w przypadku podejrzenia zachorowania i Pobieranie i obróbka materiału diagnostycznego). Zachęcamy wszystkich lekarzy do dokładnego przestudiowania tych fragmentów wytycznych.
2. Badania bakteriologiczne – nie tylko posiew. Lekarz powinien także pamiętać, że próbkę materiału klinicznego powinno się wysłać zgodnie z wytycznymi (ryc. 1.) do centralnego laboratorium referencyjnego (aktualnie KOROUN) także wówczas, gdy pomimo przekonującego obrazu klinicznego IChP (lub innego inwazyjnego zakażenia bakteryjnego) wynik standardowego posiewu płynu mózgowo-rdzeniowego (PMR) lub wysięku z jamy opłucnej wykonanego w lokalnym laboratorium jest ujemny (wg KOROUN po 24 h hodowli; szczegółowa instrukcja – p. http://koroun.edu.pl/instrukcja-wysylania-szczepow-i-materialow-do-koroun/). W polskich warunkach najczęściej musi o tym pamiętać lekarz zabezpieczając drugą próbkę referencyjną, bo z informacji zebranych „z terenu” wynika, że wiele lokalnych laboratoriów nie robi tego automatycznie. Polecamy więc wszystkim Czytelnikom, aby dokładnie zapoznali się z podanymi przez WHO zasadami właściwego przechowywania materiału diagnostycznego (p. Przechowywanie i transport) lub – jeśli jest to możliwe – ustalili odpowiednią procedurę postępowania z lokalnym laboratorium mikrobiologicznym (próbkę do wysyłki do laboratorium referencyjnego trzeba zabezpieczyć przed rozpoczęciem rutynowej diagnostyki mikrobiologicznej!).
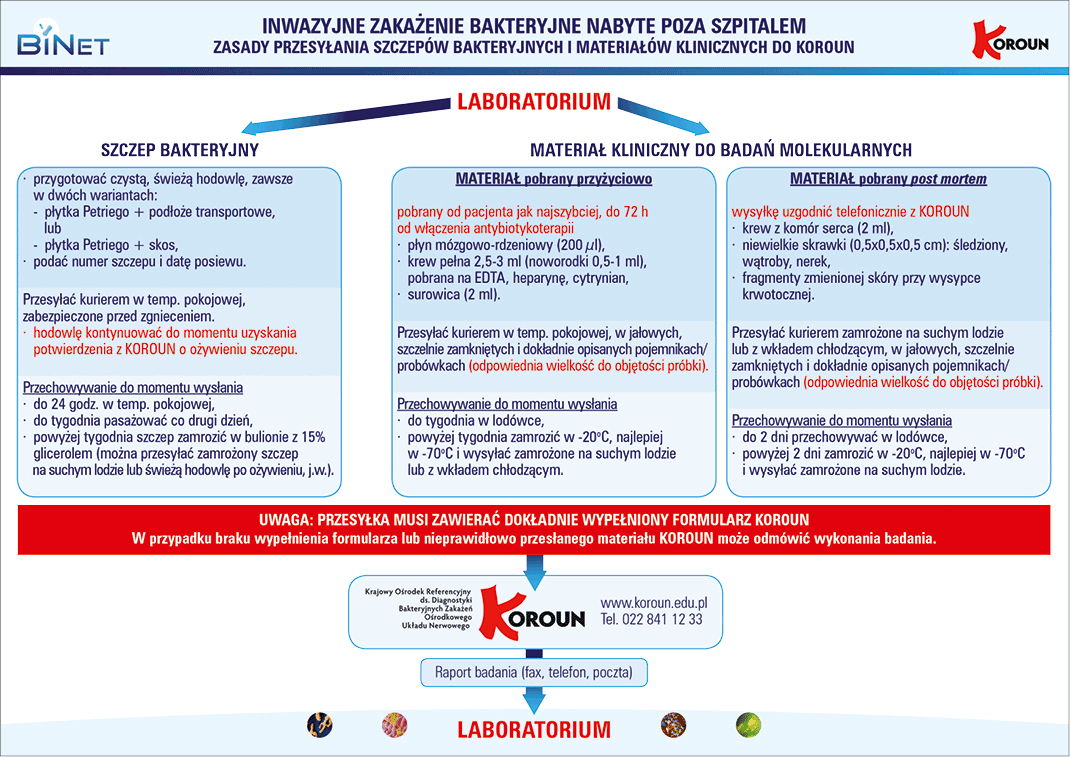
Ryc. 1. Zasady przesyłania izolatów lub materiału klinicznego do KOROUN w przypadku podejrzenia lub potwierdzonego inwazyjnego zakażenia bakteryjnego http://koroun.edu.pl/wp-content/uploads/2017/10/instrukcja-przesylania-materialow-do-Koroun.pdf [dostęp: 10.12.2019 r.])
Z zebranych przez nas informacji wynika, że szybkie
testy diagnostyczne do wykrywania pneumokoków nie
są raczej stosowane w polskich laboratoriach mikrobiologicznych w ramach rutynowej diagnostyki, dlatego w razie ujemnego wyniku posiewu PMR lub płynu z jamy
opłucnej – pomimo mocnego podejrzenia IChP zgodnie z kryteriami klinicznymi WHO – jedyną możliwością
określenia przyczyny zakażenia inwazyjnego pozostaje w wielu szpitalach wykonanie PCR w laboratorium referencyjnym
(KOROUN). W niektórych ośrodkach test
lateksowy z PMR lub test immunochromatograficzny BinaxNOW
(PMR, płyn z jamy opłucnej) wykonuje się tylko
na wyraźne zlecenie lekarza, dlatego zachęcamy wszystkich
lekarzy, aby się skontaktowali z lokalnym laboratorium
mikrobiologicznym i dowiedzieli się, jakimi
możliwościami diagnostyki IChP dysponuje i jak należy
wypełnić skierowanie (zlecenie) na badanie. W przypadku
krwi jedyną możliwością diagnostyki bakteriologicznej
jest posiew (pozostałe metody nie są wystarczająco
swoiste, zwłaszcza u dzieci).
WHO wskazuje, że w diagnostyce etiologii zapalenia
płuc u dorosłych (ale nie u dzieci) dodatkowo można
wykorzystać test do wykrywania antygenów pneumokoka w moczu. Jednak tę metodę także rzadko stosuje
się w polskich szpitalach, mimo iż zapalenie płuc jest
najczęstszą postacią kliniczną choroby pneumokokowej.
3. Badania w trakcie antybiotykoterapii. Ujemny wynik posiewu jest często konsekwencją antybiotykoterapii rozpoczętej przed pobraniem materiału do badań bakteriologicznych. Wydaje się, że w naszych warunkach jest to dość częsty scenariusz. Im dłużej trwa leczenie przeciwbakteryjne, tym mniejsze prawdopodobieństwo wyhodowania pneumokoka i tym większe znaczenie innych, niehodowlanych metod wykrywania zakażenia (PCR, ew. BinaxNOW lub inne testy antygenowe). Optymalnie materiał do badań bakteriologicznych należy pobierać przed rozpoczęciem antybiotykoterapii, ale WHO rekomenduje, aby PCR z PMR wykonać we wszystkich przypadkach podejrzenia pneumokokowego ZOMR, w których wynik posiewu jest ujemny, zwłaszcza gdy chory był już leczony antybiotykiem przed pobraniem próbki do badań. KOROUN zaleca natomiast przesyłanie materiałów pobranych w ciągu <72 h od podania pierwszej dawki antybiotyku, co może ograniczać liczbę próbek materiałów klinicznych nadsyłanych do laboratorium centralnego. W latach 2012–2018 w KOROUN metodą PCR potwierdzano tylko 16–30 (2–5%) przypadków IChP (tab. II), a zdecydowaną większość stanowiły izolaty uzyskane metodami hodowlanymi.22 Ta obserwacja potwierdza przypuszczenie, że do KOROUN zgłasza się główne przypadki, w których posiew w lokalnym laboratorium szpitala dał wynik dodatni i można przesłać izolat. Tymczasem Autorzy wieloośrodkowego badania z prospektywnym zbieraniem danych przeprowadzonego w latach 2003–2004 w 124 szpitalach i oddziałach pediatrycznych w kilku województwach w Polsce zaobserwowali, że w 108 ze 134 przypadków laboratoryjnie potwierdzonej IChP u dzieci <5. rokiem życia wynik posiewu bakteriologicznego był ujemny, a 28% chorych leczono już antybiotykiem przed pobraniem materiału do badań mikrobiologicznych.23 Ponadto, aktywne poszukiwanie przypadków przez lekarzy w tym badaniu oraz diagnostyka metodami hodowlanymi i niehodowlanymi (wykrywanie antygenów testem lateksowym, PCR) umożliwiło określenie zapadalności na pneumokokowe ZOMR u dzieci <5. roku życia na 3,8/100 000/rok, a <2. rż. na 4,1/100 000/rok,23 podczas gdy dane uzyskane w rutynowym nadzorze biernym w 2016 roku (czyli poprzedzającym wprowadzenie powszechnych szczepień PCV-10) wskazują na 2–3 razy mniejsze wartości współczynników zapadalności (odpowiednio 1,28/100 000/rok i 2,31/100 000/rok).18
Nadzór bierny vs nadzór czynny – zadania instytucji zdrowia publicznego i Ministerstwa Zdrowia
Nadzór nad IChP w Polsce ma charakter obowiązkowy,
bierny (tzn. lekarze mają prawny obowiązek zgłaszania
potwierdzonych zachorowań do odpowiednich służb
sanitarnych, ale brak mechanizmów czynnie stymulujących
wykrywalność i zgłaszalność), natomiast przesyłanie
izolatów i próbek klinicznych do KOROUN jest nadzorem
biernym, dobrowolnym (jest to wola i decyzja lekarza
opiekującego się chorym).24,25 Istotą nadzoru czynnego
(aktywnego) jest stałe stosowanie dodatkowych mechanizmów,
które ułatwiają i przypominają lekarzom o pobieraniu odpowiednich próbek do odpowiednich
badań mikrobiologicznych w każdym przypadku podejrzenia
IChP zgodnego z podanymi przez WHO kryteriami
klinicznymi (zespoły objawów klinicznych). Zasadniczą
różnicą między nadzorem biernym i czynnym jest więc
stała praca nad świadomością i organizacyjnymi (w tym
finansowymi) możliwościami lekarzy na oddziałach szpitalnych
oraz oddziałach ratunkowych (SOR), aby badania
bakteriologiczne traktować jako obowiązkowy,
rutynowy element postępowania w takich przypadkach.
Podanych przez WHO wartości wskaźników dobrej
jakości nadzoru (>80–90% pacjentów z podejrzeniem
IChP, u których wykonano odpowiednie badania bakteriologiczne
– p. Tabela. Wskaźniki skuteczności (jakości) nadzoru epidemiologicznego nad zakażeniami pneumokokowymi), nie sposób osiągnąć bez
prowadzenia nadzoru czynnego, czyli różnych metod
aktywnego, częstego komunikowania się z lekarzami w szpitalach w celu przypominania im kiedy i jak pobierać
oraz wysłać próbki do badań bakteriologicznych, bez
identyfikowania i likwidowania barier organizacyjnych
oraz finansowych utrudniających zlecanie i wykonywanie
właściwych badań mikrobiologicznych, ewentualnie
bez innych mechanizmów zwiększających automatycznie
kompletność danych (np. wewnętrzne procedury szpitalne,
system komputerowy i/lub oficjalne standardy postępowania
wymuszające pobieranie próbek i przesyłanie
ich do badań bakteriologicznych w przypadku każdego
uzasadnionego podejrzenie IChP, większa punktacja i finansowanie
dla szpitala w przypadku ustalenia etiologii
zakażenia itp.). Równoległą komunikację i przypomnienia
należy kierować do lokalnych laboratoriów mikrobiologicznych,
aby przesyłały izolaty do laboratorium centralnego
(KOROUN) i współdziałały z lekarzami na oddziałach w celu aktywnego wykrywania przypadków IChP.
Takie aktywne poszukiwanie przypadków istotnie poprawia
wykrywalność IChP, co pokazały wyniki cytowanego
powyżej polskiego badania wieloośrodkowego.23
Komentowany dokument WHO odsyła po informacje o metodach oceny efektów programu szczepień PCV
do bardziej szczegółowych wytycznych WHO z 2012
roku,26 w których czynny nadzór populacyjny nad inwazyjnymi
chorobami bakteryjnymi uznano za najdokładniejszą, a tym samym zalecaną metodę monitorowania
trendów zapadalności w czasie, umożliwiającą ocenę
bezpośrednich i pośrednich efektów programów szczepień.
Tylko nadzór populacyjny umożliwia wyliczenie
współczynników zapadalności preferowanych w ocenie
efektów programu szczepień PCV (w tym zjawiska zastępowania
serotypów; p. niżej). Istotne jest jednak precyzyjne
ustalenie tzw. populacji źródłowej (catchment
population), czyli wielkości populacji (w określonym wieku
[np. dzieci <5. rż.] lub ogólnej), z której pochodzą
chorzy z podejrzeniem IChP. Choć nadzór prowadzony w Polsce określa się jako populacyjny (teoretycznie obejmuje
całą populację kraju), to jednak z powodu małej
wykrywalności i, lub zgłaszalność przypadków IChP (nie
wszystkie szpitale aktywnie uczestniczą w nadzorze koordynowanym
przez KOROUN) nie znamy rzeczywistej
liczebności populacji, z której rekrutują się zarejestrowani
chorzy. Mała wykrywalność i teoretyczne założenie, że
nadzór realnie obejmuje całą populację Polski powodują,
że współczynniki zapadalności na IChP są w Polsce
znacznie zaniżone w porównaniu z innymi krajami o podobnym
poziomie rozwoju w Europie i na świecie (tab. I).
Nadzór populacyjny można prowadzić:
- w reprezentatywnej części populacji kraju w rejonie wybranych szpitali – jest tańszy i łatwiej zapewnić kompletność danych oraz większą czułość, ale trzeba dobrze wybrać reprezentatywną próbę z całej populacji, aby można było uogólnić wyniki na cały kraj, a poza tym szpitale powinny przyjmować odpowiednią liczbę chorych (zgodnie z kryteriami podanymi przez WHO), aby wyniki były wiarygodne; tak zorganizowany nadzór istnieje np. w Holandii13
- w całej populacji kraju – w takim przypadku trudniej zapewnić kompletność zgłoszeń i sprostać kryteriom jakości wyznaczonym przez WHO bez nadzoru czynnego lub innych mechanizmów zwiększających czułość systemu (p. wyżej; bez nich system jest nieefektywny i mało czuły, co istotnie ogranicza możliwości wiarygodnej oceny efektów programu szczepień PCV); taki rodzaj nadzoru czynnego działa np. w Wielkiej Brytanii6.
Zorganizowanie systemu czynnego nadzoru populacyjnego jest zadaniem instytucji zdrowia publicznego i rządu. Koordynacją nadzoru, analizą wyników, ich prezentacją i interpretacją powinien się zajmować zespół specjalistów, w którego skład wejdą między innymi epidemiolodzy, specjaliści zdrowia publicznego, mikrobiolodzy i lekarze klinicyści. Podobnie jak w wielu innych krajach Unii Europejskiej, Stanach Zjednoczonych czy Kanadzie to epidemiolodzy powinni odgrywać wiodącą rolę w zaplanowaniu systemu, oficjalnej prezentacji i interpretacji danych oraz okresowej ocenie jakości funkcjonowania nadzoru, bowiem dysponują odpowiednią wiedzą i umiejętnościami w tym zakresie. Nadzór epidemiologiczny to nic innego, jak jeden z wielu rodzajów badań obserwacyjnych. Mikrobiolodzy z kolei w ramach swoich kompetencji powinni dbać o wiarygodność badań mikrobiologicznych. Przykładem takiej współpracy może być ostatnia publikacja dotycząca epidemiologii pneumokokowego ZOMR w Polsce przed wprowadzeniem programu powszechnych szczepień niemowląt PCV-10.25 Przeprowadzona przez autorów tego artykułu wyważona i merytoryczna dyskusja oraz ostrożna interpretacja danych z uwzględnieniem podstawowych słabości pokazuje, jak złożonym zagadnieniem jest ocena epidemiologii IChP, jakie są istotne mankamenty polskiego systemu nadzoru (opisaliśmy je powyżej) i jak mogą one utrudniać ocenę efektów programu szczepień przeciwko pneumokokom w Polsce.
Wykorzystanie danych z nadzoru do modyfikacji programu szczepień – rozważnie i nieromantycznie
Nadzór epidemiologiczny to badanie obserwacyjne (opisowe) o charakterze ekologicznym – opisuje zaobserwowane
zjawiska w określonej populacji na przestrzeni
czasu przed wprowadzeniemu interwencji w postaci
programu szczepień oraz po jej wprowadzeniu. Wyciąganie
wniosków o związkach przyczynowo-skutkowych
(np. z programem szczepień) na podstawie takich obserwacji
wymaga daleko posuniętej ostrożności i rozległej
wiedzy. Odnotowane w czasie realizacji programu szczepień
PCV zmiany w epidemiologii IChP mogą być bowiem
wynikiem działania wielu innych znanych i nieznanych
czynników zewnętrznych (p. niżej), które są ich przyczyną
i, lub modyfikują w różnym stopniu efekty przypisywane
szczepieniom (czynniki zakłócające). Im lepszej jakości są
dane z nadzoru, tym mniejsze ryzyko, że są one wynikiem
przypadku lub błędu systematycznego.
Jednak nawet dobrej jakości nadzór nie wyeliminuje
znaczącego ryzyka błędów systematycznych, które
są immanentną cechą takiej konstrukcji metodologicznej
badania. Racjonalne próby interpretacji efektów programu
szczepień PCV na podstawie danych z nadzoru epidemiologicznego
nad IChP muszą uwzględniać całość
wiedzy w tym zakresie, w tym publikacje z innych krajów o podobnym poziomie rozwoju i sytuacji epidemiologicznej.
Poniżej przedstawiamy uwagi dotyczące interpretacji
kilku monitorowanych zazwyczaj parametrów.
1. Wpływ na zapadalność na IChP ogółem u dzieci <5. roku życia. Dzięki prowadzonym od kilku–kilkunastu lat powszechnym szczepieniom niemowląt szczepionkami skoniugowanymi – najpierw PCV-7, a potem PCV-10 lub PCV-13 – we wszystkich krajach osiągnięto znaczące zmniejszenie zapadalności na IChP ogółem w populacji dzieci <5. roku życia (tab. I). Aktualne współczynniki zapadalności w tej grupie wiekowej na podstawie ostatnich oficjalnych publikacji po co najmniej 5-letnim okresie szczepień są w zasadzie zbliżone (tab. I), mimo iż w poszczególnych krajach:
- wprowadzano szczepienia PCV w różnym czasie (8–19 lat temu)
- stosowano różne szczepionki (najpierw PCV-7, a potem PCV-10 lub PCV-13, albo od początku PCV-10) oraz różne schematy szczepień (2+1 lub 3+1)
- różny był odsetek dzieci uprawnionych do szczepień, które otrzymały zalecane dawki szczepienia pierwotnego lub podstawowego, czyli tzw. wyszczepialność (np. w Austrii przez większość lat odsetek był bardzo mały [<50%, tab. I], podczas gdy w Wielkiej Brytanii szybko osiągnięto poziom 92–94%)
- przeprowadzono dodatkowo szczepienia wychwytujące wśród starszych dzieci (np. w Stanach Zjednoczonych) lub skupiono się tylko na szczepieniach niemowląt (np. w Wielkiej Brytanii, Finlandii czy Holandii)
- zalecano oficjalnie szczepienia PCV-13 u dorosłych (Stany Zjednoczone) lub nie wydano formalnie takiego zalecenia (inne kraje wymienione w tab. I).
Między innymi z powodu powyższych różnic ocena
skuteczności PCV-10 i PCV-13 na podstawie efektów
programów szczepień w poszczególnych krajach jest
trudna i obarczona bardzo dużym ryzykiem błędu, a porównywanie
względnych efektów uzyskanych w różnych
krajach wymaga dużej ostrożności i rozległej wiedzy
epidemiologicznej. Nie jest to odpowiedni model
badawczy do oceny rzeczywistej skuteczności bezpośredniej
szczepionek, która wymaga przeprowadzenia
badań obserwacyjnych z grupą kontrolną (np. kliniczno-kontrolnych
lub kohortowych). Można je planować i przeprowadzać między innymi wykorzystując dane zgromadzone w rutynowym nadzorze epidemiologicznym, co
dodatkowo zaleca WHO w komentowanym dokumencie.
Największą względną redukcję zapadalności zaobserwowano w tych krajach, w których wartość współczynnika
wyjściowo (tzn. przed rozpoczęciem programu
szczepień) była największa, a szczepienia prowadzono
długo (tab. I). Proste porównanie współczynników zapadalności
przed wdrożeniem programu szczepień i aktualnie
po kilkunastu latach jego realizacji wskazuje jednak,
że efekt względny (% redukcji zapadalności na IChP) w populacji dzieci <5. roku życia różni się nawet w tych
państwach, w których stosowano te same szczepionki
(np. najpierw PCV-7, a potem PCV-13 – Stany Zjednoczone i Wielka Brytania vs Francja i Niemcy; tab. I). Sugeruje
to, że istotną rolę odgrywają inne czynniki zewnętrzne,
na przykład związane z odmienną charakterystyką
samej populacji (np. struktura stanu zdrowia, czynniki
ryzyka zdrowotnego, genetyczna podatność na IChP itp.). Z kolei w krajach europejskich, w których stosowano
inne szczepionki (np. w Holandii [najpierw PCV-7, potem
PCV-10] lub Finlandii [od początku tylko PCV-10]) także
uzyskano bardzo duże zmniejszenie zapadalności na IChP
ogółem u dzieci <5. rż. (tab. I).
Ponadto w krajach, w których system nadzoru nie był
dostatecznie czuły i w wybranych populacjach zapadalność
była znacząco niedoszacowana, po kilku latach realizacji
programu szczepień odnotowano paradoksalnie
większą wartość współczynników (np. w Niemczech w populacji ≥60. rż., albo w Austrii w populacji ogólnej –
p. tab. I). Jest to typowe zjawisko związane z poprawą
jakości i czułości systemu nadzoru, rosnącą świadomością
lub czujnością diagnostyczną lekarzy, a w efekcie
zwiększeniem wykrywalności chorób w trakcie realizacji
programu szczepień. Zjawisko to obserwujemy aktualnie
także w Polsce (tab. I). Niestety, mała wykrywalność
IChP przed rozpoczęciem programu powszechnych szczepień i poprawa czułości nadzoru w trakcie jego realizacji
znacznie utrudniają rzetelną ocenę efektów programu
szczepień PCV, a w najgorszym przypadku mogą zupełnie
uniemożliwić wykazanie korzystnego wpływu, nawet
jeśli w rzeczywistości on istnieje.
WHO zaleca, aby efekty programu szczepień PCV
na potrzeby jego ewentualnej modyfikacji oceniać najwcześniej
po 5 latach jego konsekwentnej realizacji.26 W Polsce powszechne szczepienia niemowląt
PCV-10 wprowadzono na początku 2017 roku, realnie
pierwsze dzieci zaczęto szczepić w marcu 2017 roku, a zatem niecałe 3 lata temu. Trudno zatem jednoznacznie
ocenić, czy zmniejszenie współczynnika zapadalności
na pneumokokowe ZOMR u dzieci do ukończenia 2. roku
życia w 2018 roku w porównaniu z 2016 rokiem o 33%
(2,31 vs 1,54/100 000/rok) jest już pierwszym zwiastunem
korzystnego wpływu powszechnych szczepień PCV,
czy też wynika z innych przyczyn.18,19 Jeśli tendencja
utrzyma się także w 2019 roku, to związek z programem
szczepień będzie bardziej prawdopodobny. ZOMR jest
zespołem klinicznym w najmniejszym stopniu podatnym
na niedoszacowanie pośród wszystkich postaci klinicznych
IChP, a rozpoznania są najbardziej wiarygodne, dlatego
WHO uznaje nadzór nad ZOMR za podstawowy
(minimalny) sposób monitorowania epidemiologii IChP.
2. Zmiany dystrybucji serotypów (zastępowanie serotypów).
WHO w swoim stanowisku z 2019 r. dotyczącym
szczepień przeciwko pneumokokom ostrzega,
że czynniki niezwiązane ze szczepionką mogą wpływać
na rejestrowane współczynniki zachorowań wywołanych
przez poszczególne serotypy, a tym samym
zakłócać interpretację związku pomiędzy wprowadzeniem
szczepień PCV a zmianami w dystrybucji
serotypów.2 Czynniki te obejmują między innymi:
zmiany w proporcji izolatów serotypowanych przed
wprowadzeniem szczepień PCV i po ich wprowadzeniu,
zmiany praktyki związanej z pobieraniem krwi
na posiew, naturalne trendy sekularne (czyli okresowe
fluktuacje częstości występowania niezwiązane
ze szczepieniami) i epidemie choroby pneumokokowej.
Należy je uwzględniać w interpretacji wyników
nadzoru epidemiologicznego nad IChP.2
W 2013 roku grupa autorów z międzynarodowej
Serotype Replacement Study Group (SRSG), po analizie
danych z 21 systemów nadzoru z różnych krajów, sformułowała
zalecenia dotyczące charakterystyki dobrej jakości
nadzoru epidemiologicznego i przedstawienia danych,
aby można było wyciągać wiarygodne wnioski na temat
zmiany dystrybucji poszczególnych serotypów pneumokoka
podczas realizacji programu szczepień PCV.27 Na tę
pozycję piśmiennictwa powołuje się komentowany przez
nas standard WHO. SRSG zaleca między innymi, aby:
- nie wyciągać wniosków na temat zastępowania serotypów w sytuacji, gdy małe zmiany w bezwzględnej liczbie izolatów (liczba w liczniku współczynnika zapadalności) powodują duże zmiany wartości współczynników zapadalności, co ma zapobiegać wyciąganiu fałszywych wniosków na podstawie niestabilnej liczby izolatów wynikającej ze zbyt małej realnej populacji źródłowej (m.in. w wyniku małej wykrywalności IChP i małej czułości systemu nadzoru); ta sama uwaga dotyczy wartości procentowych, np. zmiana w ciągu roku z 3 na 6 lub z 8 na 16 izolatów danego serotypu, to „wzrost o 100%”, ale w praktyce nie ma to żadnego znaczenia i nie pozwala wyciągać żadnych wiarygodnych wniosków
- wyliczyć i analizować współczynniki zapadalności, bo w odróżnieniu od prezentowania liczby izolatów, współczynniki zapadalności są bardziej wiarygodne i zmniejszają ryzyko błędnych wniosków spowodowanych wpływem okresowych zmian liczebności populacji źródłowej (liczba w mianowniku współczynnika zapadalności) i/lub zmiany postępowania pacjentów poszukujących pomocy lekarskiej
- wnioski dotyczące efektów programu szczepień PCV wyciągać co najmniej po 3 latach jego realizacji (wg WHO po ≥5 latach27), aby zmniejszyć ryzyko błędu spowodowanego zbyt krótkim okresem obserwacji
- bardzo ostrożnie intepretować zwiększenie współczynników zapadalności dla serotypów pozaszczepionkowych, jeśli odsetek zaszczepionych PCV w analizowanej populacji jest <70%
- regularnie oceniać system nadzoru pod kątem czułości i spójności, co umożliwia wprowadzanie poprawki we współczynnikach zapadalności związanych ze zmianami czułości systemu.
Jeszcze raz podkreślamy, że wnioskowanie o skuteczności
szczepionek u indywidualnych pacjentów
(ochrona bezpośrednia) na podstawie badań, których
celem była ocena efektów epidemiologicznych programów
szczepień, nie jest prawidłowe i często prowadzi
do wypaczonych wniosków, zwłaszcza w zakresie analizy
poszczególnych serotypów z względnie małą liczbą
zarejestrowanych przypadków.
Z powodu wymienionych zastrzeżeń metodologicznych,
na podstawie analizy danych z nadzoru epidemiologicznego
nie formułuje się żadnych zapisów w charakterystyce
produktu leczniczego (ChPL) szczepionek, a dla
instytucji zdrowia publicznego powinny one stanowić
dodatkowe źródło informacji intepretowanych zawsze w kontekście wyników oceny skuteczności poszczególnych
preparatów u indywidualnych szczepionych osób
(ochrona bezpośrednia; badania z odpowiednią grupą
kontrolną) i wobec najważniejszego kryterium skuteczności,
jakim jest zachorowanie na IChP niezależnie
od serotypu penumokoka (efekt netto, czyli wobec IChP
ogółem).
Wyniki opublikowanych do tej pory badań epidemiologicznych
wskazują, że efekt netto w postaci zmniejszenia
zapadalności na IChP ogółem w populacji objętej
szczepieniami jest podobny dla programów realizowanych
szczepionką PCV-10 lub PCV-13, i nie ma przekonujących
danych o wyższości jednej z tych szczepionek
wobec tak zdefiniowanego punktu końcowego.
Taką opinię wyrazili także eksperci WHO w stanowisku z 2019 roku.2 Co więcej, w przypadku obu szczepionek
PCV redukcja zapadalności na IChP ogółem w populacji
objętej szczepieniem (tab. I) jest bardzo podobna do ich
skuteczności ocenionej w badaniach z grupą kontrolną.28
Badania przeprowadzone w różnych krajach sugerują
jednak, że w zależności od użytej szczepionki PCV programy
szczepień wywierają presję selekcyjną na inne
serotypy „umykające” ochronie populacyjnej (pośredniej).
Zjawisko to może dotyczyć m.in. serotypu 19A w przypadku programów PCV-10, a innych serotypów
pozaszczepionkowych w przypadku programów PCV-13
(jak np. 12F, 8, 9N, 23B w Anglii i Walii, 24F i 15 B/C
we Francji lub 10A i 24F w Niemczech po kilku latach
realizacji szczepień PCV-13).6–11,29,30 Na zagadnienie
zmiany dystrybucji serotypów pod wpływem szczepień
PCV należy patrzeć całościowo i zawsze w kontekście
efektu wobec IChP ogółem, a nie ograniczać
analizy wyłącznie do wybranego serotypu (np. 19A lub
3) lub tylko serotypów uwzględnionych w szczepionce,
gdyż zachorowania wywołane przez typy „pozaszczepionkowe”
nieco uszczuplają ogólny wpływ programu
szczepień.2,3–27,30 To jest prawdopodobnie jeden z powodów,
dlaczego efekt netto (wobec IChP ogółem)
PCV-10 i PCV-13 jest podobny. Zjawisko „zastępowania
serotypów” dotyczy głównie populacji nieobjętej programem
szczepień (szczególnie >60.–65. rż.) i w mniejszym
stopniu jest wyrażone w populacji dzieci <5. roku życia
(ryc. 2.).6,13,30
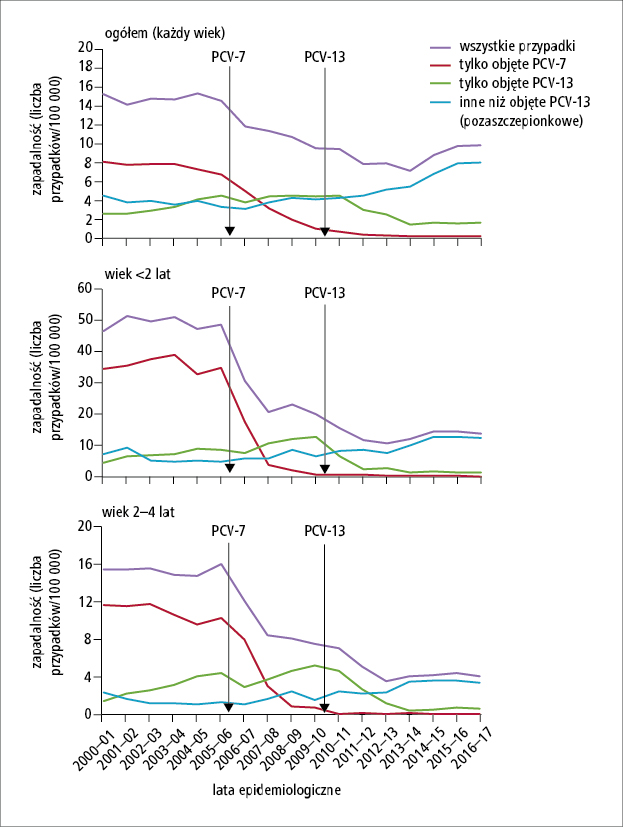
Ryc. 2. Trendy zapadalności
na inwazyjną chorobę
pneumokokową w Wielkiej
Brytanii przed i w czasie
realizacji programu
powszechnych szczepień
niemowląt przeciwko
pneumokokom w populacji
ogólnej i u dzieci (17 lat
obserwacji [na podstawie:
Ladhani S.N., Collins S.,
Djennad A. i wsp., Lancet
Infect. Dis., 2018; 18:
441–451)
3. Efekt ochrony zbiorowiskowej (pośredniej) w populacji
ogólnej. Choć WHO wskazuje, że wystarczające
dane do określenia efektów i ewentualnej
modyfikacji programu szczepień PCV można uzyskać
obejmując nadzorem populacyjnym tylko dzieci <5.
roku życia, to wyłącznie rozszerzenie nadzoru na inne
grupy wieku lub – optymalnie na całą populację –
umożliwia ocenę ochrony zbiorowiskowej (pośredniej), a dodatkowo pełniejszy wgląd w zakres zjawiska
zastępowania serotypów. Dokładne oszacowanie
ochrony zbiorowiskowej jest jednak bardzo trudne,
bo na zapadalność na IChP u osób nieobjętych
programem szczepień wpływa bardzo wiele znanych i nieznanych czynników zewnętrznych (niezwiązanych z programem szczepień), które trudno kontrolować.
Dotychczasowe obserwacje w państwach Unii Europejskiej
wskazują, że pomimo dużego efektu szczepień
PCV w populacji dzieci <5. roku życia, ochrona
pośrednia (zbiorowiskowa) populacji ogólnej przed
IChP – w tym zwłaszcza dorosłych w starszych grupach
wiekowych – po wprowadzeniu powszechnych
szczepień niemowląt PCV-10 lub PCV-13 jest niewielka
lub jej brak, głównie z powodu zwiększenia się zachorowań
wywołanych przez serotypy pozaszczepionkowe, a efekt wobec IChP ogółem nie różni się istotnie
niezależnie od zastosowanej szczepionki PCV.6–17,30
Na rycinach 2. i 3. przedstawiono zapadalność na IChP u dzieci <5. roku życia i w populacji ogólnej w Wielkiej
Brytanii i Holandii, które mają ustabilizowany od kilkunastu
lat dobrej jakości nadzór epidemiologiczny i wprowadziły
program szczepień niemowląt PCV-7 w podobnym
czasie, a następnie przeszły z tej szczepionki na PCV-13
(Wielka Brytania) lub PCV-10 (Holandia).6,13 Pomimo podobnych
efektów w zakresie zapadalności na IChP ogółem u dzieci <5. roku życia, wpływ programu szczepień
PCV-7 na ten parametr w całej populacji się różnił – o ile w Wielkiej Brytanii zaobserwowano zmniejszenie współczynnika
zapadalności, to w Holandii sytuacja praktycznie
się nie zmieniła. Tak jak zaznaczyliśmy wcześniej, może to
świadczyć o różnej charakterystyce populacji brytyjskiej i holenderskiej, dlatego bezpośrednie porównywanie
efektów programów szczepień w różnych państwach jest
trudne i powinno uwzględniać te różnice. Po zastąpieniu
PCV-7 przez PCV-13 w Wielkiej Brytanii współczynnik
zapadalności na IChP ogółem w całej populacji zmniejszył
się już bardzo nieznacznie (o 7% [IRR: 0,93; 95% CI:
0,89–0,97]), a w Holandii po wprowadzeniu PCV-10 nie
zmienił się istotnie (IRR: 1,05; 95% CI: 0,97–1,14]), w obu
przypadkach głównie z powodu zwiększenia zapadalności
na IChP wywołaną przez szczepy nieuwzględnione w PCV-13.
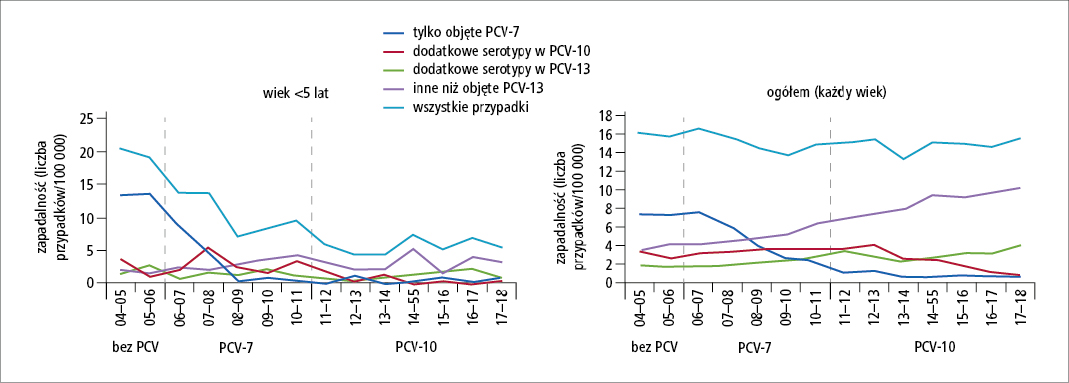
Ryc. 3. Trendy zapadalności na inwazyjną chorobę pneumokokową w Holandii przed i w czasie realizacji programu powszechnych szczepień niemowląt przeciwko pneumokokom w populacji ogólnej i u dzieci <5. rż. (12 lat obserwacji [na podstawie: Vestjens S.M.T., Sanders E.A.M., Vlaminckx B.J. i wsp.: Twelve years of pneumococcal conjugate vaccination in the Netherlands: Impact on incidence and clinical outcomes of invasive pneumococcal disease. Vaccine. 2019; 37: 6558–6565])
4. Dane kliniczne, w tym historia szczepień. Formularz
zgłoszenia do KOROUN, ale także druk zgłoszenia
zachorowania do inspekcji sanitarnej (ZLK-1) zawierają
pytanie o szczepienia, ale niestety te dane najczęściej
nie są uzupełniane przez lekarzy zgłaszających
przypadki w nadzorze lub brakuje szczegółowej informacji o rodzaju zastosowanej szczepionki, schemacie
szczepienia i dacie podania ostatniej dawki. W efekcie
aktualnie w systemie nadzoru nie ma danych o historii
szczepień nadających się do analizy. Można byłoby je
uzyskać poprzez aktywne dotarcie do dokumentacji
medycznej potwierdzonych przypadków, co zaleca
standard WHO, nawet już restrospektywnie, po potwierdzeniu
IChP i ustaleniu serotypu izolatu (pacjent
nie jest anonimowy, a formularz zgłoszenia do KOROUN
zawiera PESEL). WHO zaleca zbieranie i analizę
danych o przebytych szczepieniach, gdyż są one
przydatne w interpretacji danych z nadzoru i ocenie
efektów programu szczepień. Zwłaszcza w polskich
warunkach te dane mogą być szczególnie przydatne
ze względu dostępność różnych PCV w ramach szczepień
bezpłatnych i odpłatnych.
WHO i SRSG zalecają również, aby w analizie i prezentacji
danych uwzględniać postaci kliniczne IChP, gdyż
selektywna nadreprezentacja cięższych przypadków
(np. ZOMR) może systematycznie wypaczać dystrybucję
serotypów, a zmiana proporcji postaci klinicznych
IChP w kolejnych latach prowadzenia nadzoru
(np. w wyniku poprawy czujności diagnostycznej,
zainteresowania mediów lub praktyki pobierania lub
zlecania badań bakteriologicznych) może rzutować
na trendy zapadalności na IChP związaną z wybranymi
serotypami i zakłócać interpretację efektów programu
szczepień PCV.
Podsumowanie
Mamy nadzieję, że komentowane wytyczne WHO
udostępnione w wersji polskiej przyczynią się do dalszej istotnej poprawy
czułości i jakości systemu nadzoru nad IChP w Polsce, a problemy omówione w komentarzu wskażą lekarzom,
ekspertom i decydentom jak osiągnąć ten cel, a także
jak przedstawiać i intepretować dane z nadzoru epidemiologicznego w racjonalnej, merytorycznej dyskusji o ewentualnej potrzebie i kierunkach modyfikacji programu
szczepień przeciwko pneumokokom.
Autorzy wytycznych WHO z 2019 roku wskazują, że
nie ma badań bezpośrednio porównujących efekty kliniczne
PCV-10 i PCV-13, a inne dostępne aktualnie dane
sugerują, że obie te szczepionki są skuteczne w redukcji
IChP ogółem wywołanej przez serotypy szczepionkowe.2 Chociaż PCV-13 obejmuje 3 dodatkowe serotypy,
aktualne dane są niewystarczające, aby ocenić czy daje
to dodatkową korzyść wobec IChP ogółem.2 Zarówno
PCV-10, jak i PCV-13 wywierają bezpośredni i pośredni
efekt ochronny wobec zapalenia płuc, ale nie ma dowodów
wskazujących, że się on różni.2 Skoro efekty i skuteczność
rzeczywista obu szczepionek wobec wspólnych
serotypów szczepionkowych jest podobna, a dostępne
dowody na wyższość któregokolwiek produktu są niewystarczające,
to zgodnie z powszechnie uznanymi w medycynie
zasadami, przyjmuje się, że efekt jest podobny,
dopóki w przekonujący sposób nie zostanie udowodniona
przewaga którejkolwiek szczepionki.
Piśmiennictwo:
1. Surveillance standards for vaccine-preventable diseases, second edition. Chapter 17: Pneumococcus. Geneva: WHO; 2018: www.who.int/immunization/monitoring_surveillance2. Pneumococcal conjugate vaccines in infants and children under 5 years of age: WHO position, February 2019: www.who.int/wer/2019/wer9408/en/
3. Active Bacterial Core Surveillance (ABCs) Report Emerging Infections Program Network Streptococcus pneumoniae, 1999. www.cdc.gov/abcs/reports-findings/survreports/spneu99.pdf
4. Active Bacterial Core Surveillance (ABCs) Report Emerging Infections Program Network Streptococcus pneumoniae, 2017. www.cdc.gov/abcs/reports-findings/survreports/spneu17.pdf
5. Matanock A., Lee G., Gierke R. i wsp.: Use of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine among adults aged ≥65 years: updated recommendations of the advisory committee on immunization practices. MMWR, 2019; 68: 1069–1075
6. Ladhani S.N., Collins S., Djennad A. i wsp.: Rapid increase in non-vaccine serotypes causing invasive pneumococcal disease in England and Wales, 2000–17: a prospective national observational cohort study. Lancet Infect Dis. 2018; 18: 441–451
7. Weinberger R., von Kries R., van der Linden M. i wsp.: Invasive pneumococcal disease in children under 16 years of age: Incomplete rebound in incidence after the maximum effect of PCV13 in 2012/13 in Germany. Vaccine. 2018; 36(4): 572–577
8. van der Linden M., Imöhl M., Perniciaro S. i wsp.: Limited indirect effects of an infant pneumococcal vaccination program in an aging population. PLoS One. 2019; 14: e0220453. doi: 10.1371/journal.pone.0220453
9. Lepoutre A., Varon E., Georges S. i wsp.: Impact of the pneumococcal conjugate vaccines on invasive pneumococcal disease in France, 2001–2012. Vaccine, 2015; 33: 359–366
10. Savulescu C. Krizova P., Lepoutre A. i wsp.: Effect of high-valency pneumococcal conjugate vaccines on invasive pneumococcal disease in children in SpIDnet countries: an observational multicentre study. Lancet Respir Med., 2017; 5 (8): 648–656
11. ECDC. Invasive pneumococcal disease – Annual Epidemiological Report for 2017. www.ecdc.europa.eu
12. EPIBAC. Bulletin du réseau de surveillance des infections invasives bactériennes. www.santepubliquefrance.fr
13. Vestjens S.M.T., Sanders E.A.M., Vlaminckx B.J. i wsp.: Twelve years of pneumococcal conjugate vaccination in the Netherlands: Impact on incidence and clinical outcomes of invasive pneumococcal disease. Vaccine. 2019; 37: 6558–6565
14. National Infectious Disease Register, National Institute for Health and Welfare, THL. https://thl.fi/documents
15. Rinta-Kokko H., Palmu A.A., Auranen K. i wsp.: Long-term impact of 10-valent pneumococcal conjugate vaccination on invasive pneumococcal disease among children in Finland. Vaccine. 2018; 36: 1934–1940
16. Richter L., Schmid D., Kanitz E.E. i wsp.: Invasive pneumococcal diseases in children and adults before and after introduction of the 10-valent pneumococcal conjugate vaccine into the Austrian national immunization program. PLoS One. 2019; 14: e0210081. doi: 10.1371/journal.pone.0210081
17. ECDC. Invasive pneumococcal disease – Annual Epidemiological Report for 2014. www.ecdc.europa.eu
18. NIZP-PZH. Choroby zakaźny i zatrucia w Polsce w 2016 roku. wwwold.pzh.gov.pl
19. NIZP-PZH. Choroby zakaźny i zatrucia w Polsce w 2018 roku. wwwold.pzh.gov.pl
20. KOROUN. Inwazyjna choroba pneumokokowa (IChP) w Polsce w 2016 roku. http://koroun.edu.pl
21. KOROUN. Inwazyjna choroba pneumokokowa (IChP) w Polsce w 2018 roku. http://koroun.edu.pl
22. KOROUN: Dane epidemiologiczne. http://koroun.edu.pl/dane-epidemiologiczne
23. Grzesiowski P., Skoczyńska A., Albrecht P. i wsp.: Invasive pneumococcal disease in children up to 5 years of age in Poland. Eur. J. Clin. Microbiol. Infect. Dis., 2008; 27: 883–885
24. Skoczyńska A., Kuch A., Sadowy E. i wsp.: Recent trends in epidemiology of invasive pneumococcal disease in Poland. Eur. J. Clin. Microbiol. Infect. Dis., 2015; 34: 779–787
25. Polkowska A., Skoczyńska A., Paradowska-Stankiewicz I. i wsp.: Pneumococcal meningitis before the introduction of 10-valent pneumococcal conjugate vaccine into the National Childhood Immunization Program in Poland. Vaccine, 2019; 37: 1365–1373
26. WHO: Measuring impact of Streptococcus pneumoniae and Haemophilus influenzae type b conjugate vaccination. 2012, http://apps.who.int
27. Feikin D.R., Kagucia E.W., Loo J.D. i wsp.: Serotype-specific changes in invasive pneumococcal disease after pneumococcal conjugate vaccine introduction: a pooled analysis of multiple surveillance sites. PLoS Med., 2013; 10 (9): e1001517; doi:10.1371/journal. pmed.1001517
28. Wysocki J.: Co wiadomo o skuteczności skoniugowanych szczepionek przeciwko pneumokokom? www.mp.pl/szczepienia/ekspert
29. Levy C., Ouldali N., Caeymaex L i wsp.: Diversity of serotype replacement after pneumococcal conjugate vaccine implementation in Europe. J. Pediatr., 2019; 213: 252–253.e3
30. Hanquet G., Savulescu C, SpIDnet/I-MOVE: Indirect effect of infant PCV10/13 vaccination on IPD in the elderly: polled analysis from 13 EU sites. www.slideshare.net/ECDC_EU/germaine-hanquet-indirect-effect-of-infant-pcv1013-vaccination-on-ipd-in-the-elderlypooled-analysis-from-13-eu-sites (dostęp 02.12.2019 r.)


























