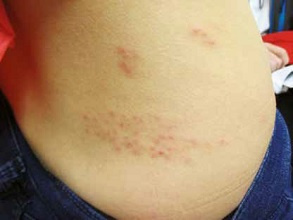
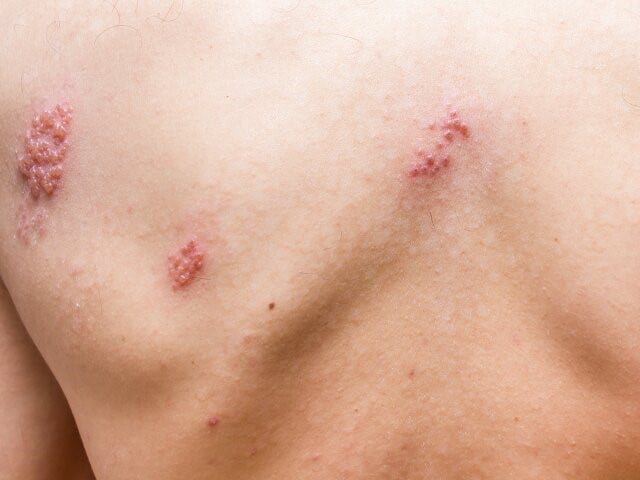
Narodowy Instytut Zdrowia Publicznego-Państwowy Zakład Higieny (NIZP-PZH) poinformował w serwisie Facebook („Szczepienia.info”), że zwolnił do obrotu pierwszą serię szczepionki przeciwko półpaścowi. Oznacza, to że już niedługo preparat ten pojawi się w aptekach.
Szczepionka przeciwko półpaścowi – Shingrix – to preparat rekombinowany, z adiuwantem. Europejska Agencja Leków (EMA) zarejestrowała szczepionkę w krajach Unii Europejskiej w marcu 2018 roku, ale do tej pory nie była ona dostępna na polskim rynku. Podstawowe informacje o szczepionce podsumowano w tabeli. Aktualna Charakterystyka Produktu Leczniczego Shingrix dostępna jest na stronie EMA (p. www.ema.europa.eu/en/medicines/human/EPAR/shingrix#product-information-section).
| Tabela. Podstawowe informacje dotyczące rekombinowanej szczepionki przeciwko półpaścowia | |
|---|---|
| Rodzaj preparatu (technologia) | rekombinowany, z adiuwantem (należy do kategorii tzw. nieżywych) |
| Wskazania do stosowania | profilaktyka półpaśca i nerwobólu popółpaścowego u dorosłych w wieku ≥50 lat oraz osób w wieku ≥18 lat należących do grup ryzyka zachorowania na półpasiec |
| Przeciwwskazania | nadwrażliwość na jakikolwiek składnik szczepionki lub po podaniu poprzedniej dawki szczepionki |
| Schemat szczepienia i droga podania | 2 dawki w schemacie 0, 2 miesiące, domięśniowo |
| Skuteczność szczepienia | 1) u osób w wieku ≥50 lat w okresie obserwacji śr. 4 lat:
|
| Tolerancja i bezpieczeństwo | najczęściej zgłaszanymi zdarzeniami niepożądanymi były: ból w miejscu wstrzyknięcia, ból mięśni, zmęczenie, ból głowy; większość miała łagodne lub umiarkowane nasilenie i utrzymywała się 2–3 dni |
| Postać farmaceutyczna | przed rekonstytucją: proszek (koloru białego) i zawiesina do sporządzania zawiesiny do wstrzykiwań (opalizujący płyn, bezbarwny/lekko brązowawy) |
| Skład jakościowy i ilościowy | 1 dawka (0,5 ml) zawiera (po rekonstytucji):
|
| Substancje pomocnicze |
|
| Warunki przechowywania |
|
| a Opracowano na podstawie 1.–4. pozycji piśmiennictwa. b Wytworzono z zastosowaniem technologii rekombinacji DNA. c Analiza post-hoc | |
Piśmiennictwo:
1. Charakterystyka produktu Leczniczego Shingrix. https://www.ema.europa.eu/en/documents/product-information/shingrix-epar-product-information_pl.pdf (dostęp: 14.03.2022)2. Lal H., Cunningham A.L., Godeaux O. i wsp: Efficacy of an adjuvanted herpes zoster subunit vaccine in older adults. N. Engl. J. Med. 2015; 372 (22): 2087–2096
3. Cunningham A.L., Lal H., Kovac M. i wsp.: Efficacy of the herpes zoster subunit vaccine in adults 70 years of age or older. N. Engl. J. Med. 2016; 375 (11): 1019–1032
4. Bastidas A., de la Serna J., El Idrissi M. i wsp.: Effect of recombinant zoster vaccine on incidence of herpes zoster after autologous stem cell transplantation: a randomized clinical trial. JAMA. 2019; 322 (2): 123–133